文 | 环球
编辑 | 小策
最近有个做短视频的朋友愁坏了,他把半年前的爆款视频重新发了一遍,结果直接被平台判了搬运,流量一夜归零。
他纳闷,“都是我自己拍的视频,怎么就成搬运了?”

这事儿实则不少创作者都遇到过,平台算法目前对“重复内容”的识别越来越严,哪怕是自己的旧视频,处理不好照样限流。
算法怎么认出“搬运货”?三个“火眼金睛”的招数
你可以把MD5值理解成视频的“电子身份证”。
每个视频文件经过算法计算,都会生成一串独一无二的字符串。

就像你身份证号一辈子不变,视频只要原封不动,MD5值也不会变。
平台后台一比对,发现半年前有个一模一样的“身份证”,直接就标上“搬运嫌疑”。
光看单个视频还不够,平台目前玩起了“连坐”。

要是你用同一个WiFi登录新旧两个号,发的视频画风又差不多,系统可能直接把新号也标成“可疑账号”。
之前有个矩阵号团队,30多个号用同一个IP发内容,结果一夜之间全被封了,连申诉的机会都没有。
这两年算法识别技术又升级了。

以前改改MD5值还能混过去,目前平台会“逐帧分析”。
列如你从别人视频里截了10秒画面,哪怕加了滤镜,系统也能通过画面构图、色彩分布认出这部分内容,直接判定“二次剪辑搬运”。
4个“改头换面”小技巧,5分钟让视频“变脸”
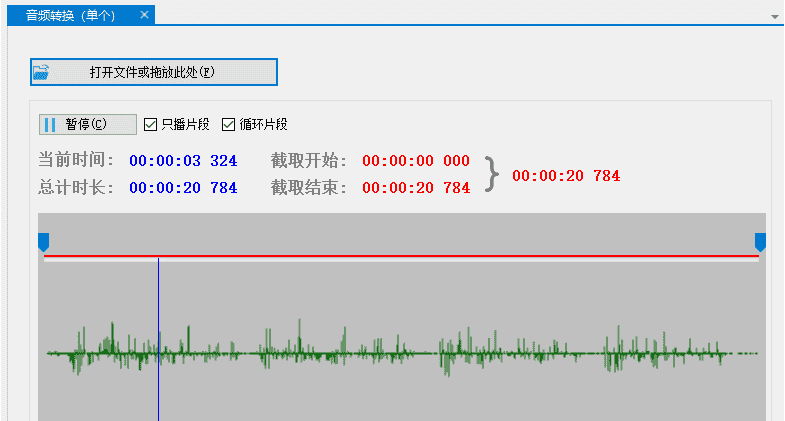
最简单的一招就是“掐头去尾”。

剪开头0.3秒黑屏,结尾0.2秒多余画面,就这么一点点改动,MD5值就会彻底变样。
我那朋友后来试了这招,同样的视频,流量直接从0涨到了5万,你说神不神。
给视频加个5%透明度的“自然”滤镜。
别选太夸张的,不然画质糊了没人看。
再把帧率从30帧调到25帧,编码结构一变,算法就认不出来了。

有个做宠物号的博主,靠这两招把旧视频重发了10条,条条都过审,还出了3个小爆款。
要是视频里没文字,直接镜像翻转一下。
画面左右反过来,系统会觉得是新视频。
但要是有LOGO或者字幕,得先把文字抹掉再翻转,不然字是反的,观众看着不舒服。

之前有个美妆博主没注意,翻转后口红品牌名是反的,评论区全在问“这啥牌子,字都印反了?”
剪映里操作顺序很重大。
先裁剪首尾,再调画布大小(放大1%就行),然后加滤镜,最后改帧率或镜像。
导出时选H.265编码,1080P分辨率,文件就彻底“换了身份”。

我自己试过,同一个视频按这个流程改完,在抖音后台检测,显示“原创度98%”。
说到底,这些微调技巧只能救急。
总靠改视频混日子,早晚被算法盯上。
去年有个美食号,靠微调旧视频涨粉10万,结果三个月后被平台清号,之前的努力全白费。
真正能长久的,还是得拍新内容。
隔壁做手工教程的老李,坚持每周拍新内容,虽然前半年没流量,但去年进了平台的“新锐创作者池”,目前每条视频都有保底5万播放。
平台算法实则不傻,你是真原创还是“改头换面”,时间长了一眼就能看出来。

目前短视频行业越来越卷,光靠“小机智”躲算法肯定不行。
不如把心思放在内容上,找到自己的独特风格。
列如有人专门拍“农村老人用传统手艺修农具”,有人专注“职场新人省钱小技巧”,这些垂直领域的原创内容,平台不仅不会限流,还会主动给流量扶持。

最后给创作者提个醒,微调技巧是“护身符”,不是“救命稻草”。
偶尔用它盘活旧内容没问题,但长期还是得靠原创。
毕竟观众刷短视频,看的是新鲜事、新观点,老是重复发旧东西,就算过了算法审核,观众也会看腻的。
相关文章